Lt304888.ru
Туристические услуги
Рекомендуем
Нитрат аммония
27-05-2023
| Нитрат аммония | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат аммония |
| Химическая формула | NH4NO3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдый |
| Отн. молек. масса | 80,04 а. е. м. |
| Молярная масса | 80,04 г/моль |
| Плотность | 1,725 (IV модификация) г/см³ |
| Термические свойства | |
| Температура плавления | 169,6 °C |
| Температура кипения | 235 °C |
| Температура разложения | ~210 °C |
| Химические свойства | |
| Растворимость в воде | 20 °C — 190 г/100 мл |
| Классификация | |
| Рег. номер CAS | 6484-52-2 |
Нитра́т аммо́ния (аммонийная (аммиачная) селитра) — химическое соединение NH4NO3, соль азотной кислоты. Впервые получена Глаубером в 1659 году.
Содержание |
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при повышенном давлении — 235 °C. Молекулярная масса 80,04 а. е. м.. Скорость детонации 2570 м/с.
Растворимость
Растворимость в воде:
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 25 | 212 |
| 50 | 346 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Также соль растворима в аммиаке, пиридине, метаноле, этаноле.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём () получить практически невозможно.
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
- при давлении, высокой температуре и катализаторе
- .
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
- Природный фосфат кальция (апатит) растворяют в азотной кислоте:
- .
- Полученную смесь охлаждают до 0 °C, при этом нитрат кальция кристаллизуется в виде тетрагидрата — Ca(NO3)2·4H2O, и его отделяют от фосфорной кислоты.
- На полученный нитрат кальция и неудалённую фосфорную кислоту действуют аммиаком, и в итоге получают нитрат аммония:
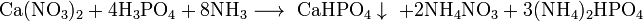 .
.
А также амфотерный метод.
Химические свойства
Реакции разложения
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
- Температура ниже 270 °C:
- .
- Температура выше 270 °C, или детонация:
- .
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) |
|---|---|---|---|
| — | > 169.6 | жидкость | |
| I | 169.6 — 125.2 | кубическая | +2.1 |
| II | 125.5 — 84.2 | тетрагональная | −1.3 |
| III | 84.2 — 32.3 | α-ромбическая | +3.6 |
| IV | 32.3 — −16.8 | β-ромбическая | −2.9 |
| V | < −16.8 | тетрагональная |
Фазовый переход от IV к III при 32,3 °C приносит неприятности производителям удобрений, потому как изменения плотности приводят к разрушению частиц при хранении и применении. Это особенно важно в тропических странах, где нитрат аммония испытывает циклические изменения, приводящие к разрушению гранул, слёживанию, повышенному пылению и риску возникновения взрыва.
Применение
Взрывчатые вещества
Наиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси:
- составы типа аммиачная селитра/дизельное топливо (АСДТ)
- жидкая смесь аммиачная селитра/гидразин (Астролит)
- водонаполненные промышленные взрывчатые вещества (Акванал, Акванит и др.)
- смеси с другими взрывчатыми веществами (Аммонит, Детонит и др.)
- Смесь с алюминиевой пудрой (аммонал)
Удобрения
Бо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений.
Аварии и взрывы
- 21 сентября 1921 года в Оппау в Германии на складе завода фирмы BASF при работах по дроблению небольшими взрывами слежавшихся масс нитрата аммония произошёл катастрофический взрыв примерно 4500 тонн удобрения и мощностью в 1-2 килотонны тротилового эквивалента. На месте склада образовалась воронка удлинённой формы размером более 160 метров и глубиной более 10 метров. По официальным данным, в результате взрыва погиб 561 человек[1].
- 16 апреля 1947 года во время погрузки аммиачной селитры на пароход «Гранкан» в гавани города Техас-сити (англ.) произошёл пожар, который в результате неграмотных действий по его тушению, привёл к катастрофическому по последствиям взрыву приблизительно 2300 тонн удобрения. В результате взрыва были разрушены портовые сооружения, несколько судов, многие предприятия и жилые дома. Погибло более полутора тысяч человек, сотни пропали без вести и их тела не были найдены. Травмы получили более трёх с половиной тысяч человек.[2]
- 22 июля 2011 год в Правительственном квартале Осло, Норвегия, прогремел взрыв. Заложенная в автомобиль «Volkswagen Crafter» радиоуправляемая бомба была изготовлена из сельскохозяйственных удобрений на основе аммиачной селитры и дизельного топлива. Вследствии этого взрыва 8 человек погибли, пятнадцать получили ранения. Виновником теракта был объявлен Андерс Беринг Брейвик
Дополнительная информация
Мировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот.
См. также
Примечания
- Взрыв по аутсорсингу // Бизнес-журнал. — 20 мая 2007. — № 10.
- Пожар и взрыв на Гранкане
- Взрыв грузовика в Испании на Podrobnosti.ua(недоступная ссылка)
Ссылки
- Нитрат аммония в химическом словаре
Литература
- Технология аммиачной селитры, под ред. В. М. Олевского, М., 1978.
- Соли азотной кислоты, Миниович М. А., М., 1964.
- Олевский В. М., Ферд М. Л., «Ж. Всес. хим. о-ва им. Д. И. Менделеева», 1983, т. 28, № 4, с. 27—39.
Нитрат аммония.
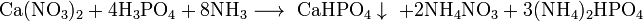 .
.